【文献解读】血浆置换与双重血浆分子吸附系统单用或联合使用治疗HBV相关慢加急性肝衰竭患者预后预测模型的建立与评估
发布时间:2022-11-08

【文献导读】
目前对于肝衰竭患者的预后评价主要采用MELD和MELD-Na评分,但这些评分是否适用于接HBV-ACLF患者的预后尚不明确。安徽医科大学省立医院和安徽医科大学第二附属医院回顾性分析了进行PE、DPMAS及DPMAS+PE治疗HBV-ACLF患者的24周生存预后的独立影响因素,建立了一种新的生存预测模型,并对新建立的预测模型进行了验证。本文献原文于2021年发表在《临床肝胆病杂志》上。

01 对象与方法 研究对象 收集2015 年1月-2019年12月在安徽医科大学附属省立医院接受PE+ DPMAS 治疗的HBV-ACLF患者为建模组,另收集2018 年1月-2020 年1 月在安徽医科大学第二附属医院接受PE+DPMAS 治疗的HBV-ACLF患者为验证组。所有的患者除接受PE+DPMAS外,均接受针对HBV-ACLF的内科综合治疗,包括口服抗病毒药物、保肝降酶、输白蛋白等对症治疗。
研究方法 建模组患者133例和验证组患者55例实行PE+DPMAS治疗,收集临床资料、检测结果及并发症情况,同时计算MELD及MELD-Na评分。运用Cox回归分析进行单因素及多因素分析,确定主要影响因素,建立预测模型。绘制受试者特征曲线(ROC曲线),采用DeLong法比较新的预测模型和MELD及MELD-Na评分的ROC曲线下面积(AUC)。

02 研究结果 一般资料
建模组患者的INR(P=0.001 )、Cr(P<0.001)均高于验证组患者,同时验证组患者的MELD(P<0.001)和MELD-Na(P=0.002)评分均低于建模组患者。2 组患者其他指标比较,差异均无统计学意义(P 值均>0.05)。
患者24周生存率的影响因素分析 根据24周的生存情况,将建模组患者分为生存组(n=71)和死亡组(n=62)(表2)。生存组患者较死亡组患者更为年轻(P<0.001)。死亡组合并有肝肾综合征(P=0.005)、肝性脑病(P =0.002)、消化道出血(P=0.008)的患者较生存组多。死亡组患者的TBil (P=0.001)、INR(P<0.001)和Cr(P=0.015)较生存组高。死亡组患者的Alb(P=0.035)和PLT(P=0.002)水平较生存组低。根据Cox回归分析显示,年龄、TBIL、TNR和PLT是患者24周生存的独立影响因素。
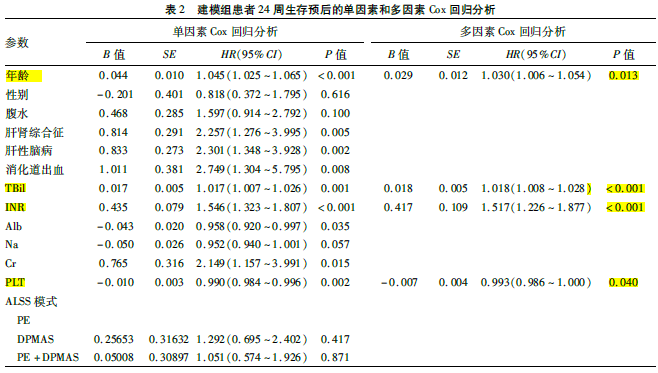
表2 建模组患者24周生存预后的单因素与多因素Cox回归分析
患者24周生存预测模型的建立
根据Cox多因素分析结果,建立了实行PE+DPMAS治疗HBV-ACLF患者的预后模型(ATIP)=0.029×年龄(岁)+0.018×TBIL(mg/dL)+0.417×INR-0.007×PLT(109/L)。建模组ATIP模型的AUC显著高于MELD和MELD-Na评分。建立的预测模型在验证组进行进一步验证,与建模组一致,ATIP模型在所有预后模型中AUC最高(图1,表3)。
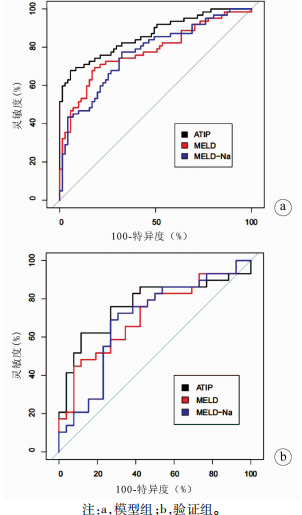
图1:不同预后模型预测HBV-ACLF患者24周生存的ROC曲线
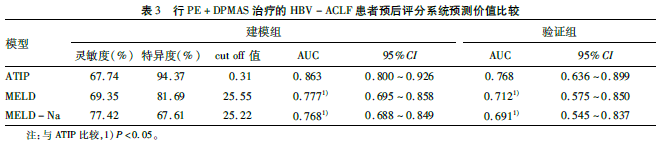
表3 行PE+DPMAS治疗的HBV-ACLF患者预后评分系统预测价值比较

03 结论 实行PE+DPMAS治疗的HBV-ACLF患者的年龄、TBIL、INR和PLT为24周生存的独立影响因素;ATIP模型对实行PE+DPMAS治疗的HBV-ACLF患者的24周预后预测效能良好。
另外,与未纳入研究的其他肝衰竭评分系统,如CTP评分、SOFA评分、APACHE评分等相比,ATIP模型具有指标客观、临床以获取和计算相对简单的等优点,因此更适合我国的临床实际。
*图源自文献,本文仅作学术交流使用
【参考文献】
黄贝贝,宁玲,李文渊,郑晓玮,张玥,江守伟,张振华,李磊.血浆置换与双重血浆分子吸附系统单用或联合使用治疗HBV 相关慢加急性肝衰竭患者预后预测模型的建立与评估[J].临床肝胆病杂志,2021,37(12): 2802-2807.
END

【文献导读】
目前对于肝衰竭患者的预后评价主要采用MELD和MELD-Na评分,但这些评分是否适用于接HBV-ACLF患者的预后尚不明确。安徽医科大学省立医院和安徽医科大学第二附属医院回顾性分析了进行PE、DPMAS及DPMAS+PE治疗HBV-ACLF患者的24周生存预后的独立影响因素,建立了一种新的生存预测模型,并对新建立的预测模型进行了验证。本文献原文于2021年发表在《临床肝胆病杂志》上。

收集2015 年1月-2019年12月在安徽医科大学附属省立医院接受PE+ DPMAS 治疗的HBV-ACLF患者为建模组,另收集2018 年1月-2020 年1 月在安徽医科大学第二附属医院接受PE+DPMAS 治疗的HBV-ACLF患者为验证组。所有的患者除接受PE+DPMAS外,均接受针对HBV-ACLF的内科综合治疗,包括口服抗病毒药物、保肝降酶、输白蛋白等对症治疗。
建模组患者133例和验证组患者55例实行PE+DPMAS治疗,收集临床资料、检测结果及并发症情况,同时计算MELD及MELD-Na评分。运用Cox回归分析进行单因素及多因素分析,确定主要影响因素,建立预测模型。绘制受试者特征曲线(ROC曲线),采用DeLong法比较新的预测模型和MELD及MELD-Na评分的ROC曲线下面积(AUC)。

一般资料
建模组患者的INR(P=0.001 )、Cr(P<0.001)均高于验证组患者,同时验证组患者的MELD(P<0.001)和MELD-Na(P=0.002)评分均低于建模组患者。2 组患者其他指标比较,差异均无统计学意义(P 值均>0.05)。
根据24周的生存情况,将建模组患者分为生存组(n=71)和死亡组(n=62)(表2)。生存组患者较死亡组患者更为年轻(P<0.001)。死亡组合并有肝肾综合征(P=0.005)、肝性脑病(P =0.002)、消化道出血(P=0.008)的患者较生存组多。死亡组患者的TBil (P=0.001)、INR(P<0.001)和Cr(P=0.015)较生存组高。死亡组患者的Alb(P=0.035)和PLT(P=0.002)水平较生存组低。根据Cox回归分析显示,年龄、TBIL、TNR和PLT是患者24周生存的独立影响因素。
表2 建模组患者24周生存预后的单因素与多因素Cox回归分析
患者24周生存预测模型的建立
根据Cox多因素分析结果,建立了实行PE+DPMAS治疗HBV-ACLF患者的预后模型(ATIP)=0.029×年龄(岁)+0.018×TBIL(mg/dL)+0.417×INR-0.007×PLT(109/L)。建模组ATIP模型的AUC显著高于MELD和MELD-Na评分。建立的预测模型在验证组进行进一步验证,与建模组一致,ATIP模型在所有预后模型中AUC最高(图1,表3)。
图1:不同预后模型预测HBV-ACLF患者24周生存的ROC曲线
表3 行PE+DPMAS治疗的HBV-ACLF患者预后评分系统预测价值比较

实行PE+DPMAS治疗的HBV-ACLF患者的年龄、TBIL、INR和PLT为24周生存的独立影响因素;ATIP模型对实行PE+DPMAS治疗的HBV-ACLF患者的24周预后预测效能良好。
另外,与未纳入研究的其他肝衰竭评分系统,如CTP评分、SOFA评分、APACHE评分等相比,ATIP模型具有指标客观、临床以获取和计算相对简单的等优点,因此更适合我国的临床实际。
*图源自文献,本文仅作学术交流使用
【参考文献】
黄贝贝,宁玲,李文渊,郑晓玮,张玥,江守伟,张振华,李磊.血浆置换与双重血浆分子吸附系统单用或联合使用治疗HBV 相关慢加急性肝衰竭患者预后预测模型的建立与评估[J].临床肝胆病杂志,2021,37(12): 2802-2807.



